
Весь контент iLive перевіряється медичними експертами, щоб забезпечити максимально можливу точність і відповідність фактам.
У нас є строгі правила щодо вибору джерел інформації та ми посилаємося тільки на авторитетні сайти, академічні дослідницькі інститути і, по можливості, доведені медичні дослідження. Зверніть увагу, що цифри в дужках ([1], [2] і т. д.) є інтерактивними посиланнями на такі дослідження.
Якщо ви вважаєте, що який-небудь з наших матеріалів є неточним, застарілим або іншим чином сумнівним, виберіть його і натисніть Ctrl + Enter.
Уточнення клітинних механізмів пародонтиту з поліпшеною моделлю на тваринах
Останній перегляд: 02.07.2025
 ">
">Дослідники з Токійського медичного та стоматологічного університету (TMDU) розробили методику, яка дозволяє детально проаналізувати розвиток пародонтиту з часом.
Пародонтит, захворювання пародонту, є основною причиною втрати зубів і вражає майже кожного п'ятого дорослого у світі. У більшості випадків цей стан виникає внаслідок запальної реакції на бактеріальну інфекцію тканин навколо зубів.
У міру погіршення стану ясна починають відступати, оголюючи коріння зубів і кістку. Примітно, що захворюваність на пародонтит зростає з віком, і оскільки населення світу живе довше, важливо мати чітке розуміння його основних причин та прогресування.
У дослідженні, опублікованому в журналі Nature Communications, дослідники з TMDU знайшли спосіб досягти цієї мети, удосконаливши широко використовувану тваринну модель для вивчення пародонтиту.
Безпосереднє вивчення пародонтиту у людей є складним. В результаті вчені часто звертаються до моделей на тваринах для доклінічних досліджень. Наприклад, «модель пародонтиту, індукованого лігатурами, на мишах» дозволила дослідникам вивчити клітинні механізми, що лежать в основі цього стану, з моменту її появи у 2012 році.
Простіше кажучи, ця модель штучно викликає захворювання пародонту, розміщуючи шовкові нитки на молярах мишей, що призводить до накопичення зубного нальоту. Хоча цей метод зручний та ефективний, він не відображає повної картини пародонтиту.
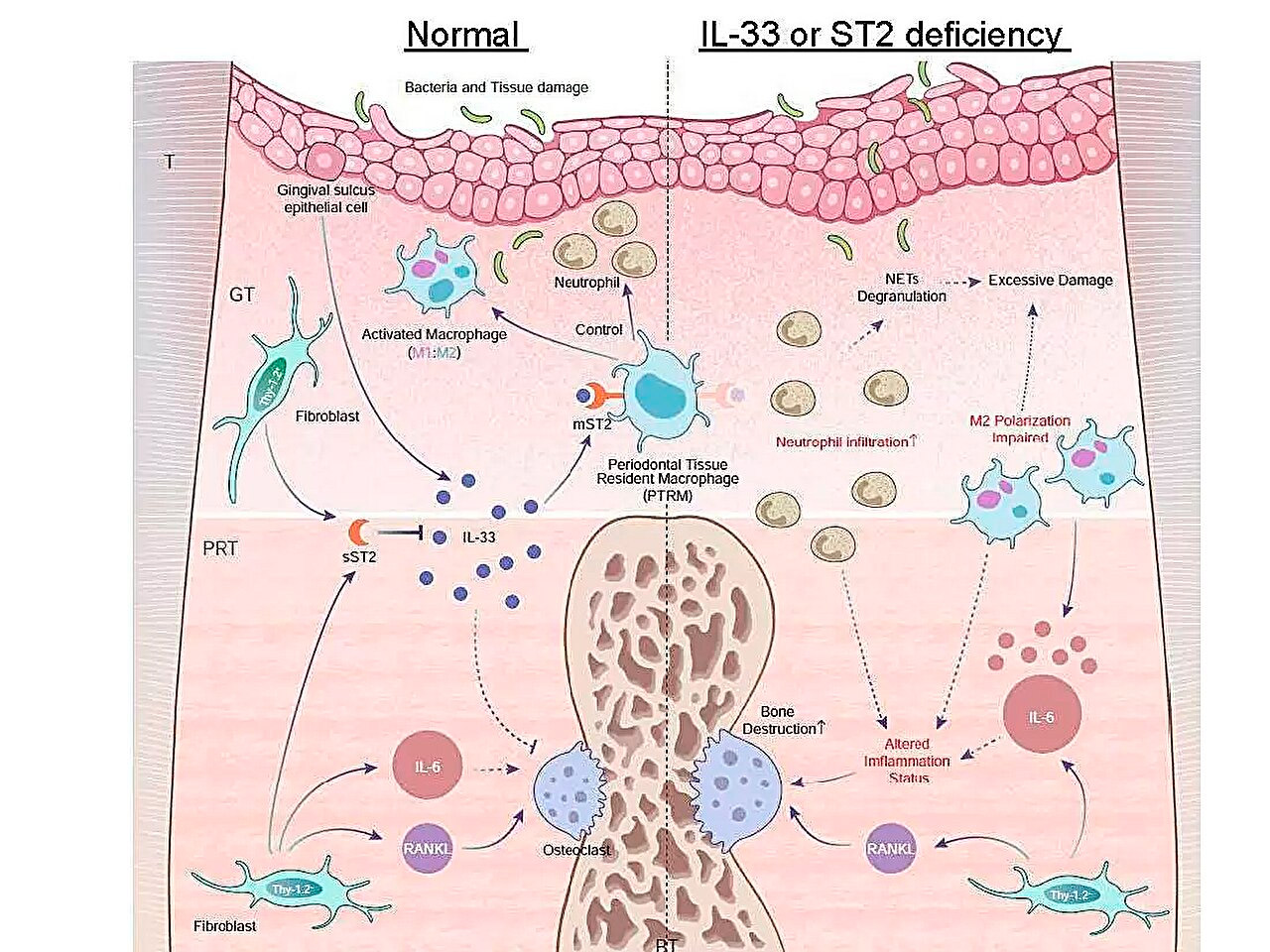
Схематичне зображення профілів експресії генів запалення під час пародонтиту та роль осі IL-33/ST2 у боротьбі з гострим запаленням. Джерело: Токійський медичний та стоматологічний університет.
«Хоча тканина пародонту складається з ясен, пародонтальної зв’язки, альвеолярної кістки та цементу, аналіз зазвичай проводиться виключно на зразках ясен через технічні та кількісні обмеження», – зазначає провідний автор дослідження Аньхао Лю. «Така стратегія відбору проб обмежує висновки, які можна зробити з цих досліджень, тому необхідні методи, що дозволяють одночасний аналіз усіх компонентів тканини».
Щоб усунути це обмеження, дослідницька група розробила модифіковану модель пародонтиту, індукованого лігатурою. Замість класичної одинарної лігатури вони використали потрійну лігатуру на верхньому лівому молярі самців мишей. Ця стратегія розширила зону втрати кісткової тканини без значного руйнування кістки навколо другого моляра, збільшуючи кількість різних типів тканин пародонту.
«Ми виділили три основні типи тканин та оцінили вихід РНК між двома моделями. Результати показали, що модель з потрійним лігуванням ефективно збільшила вихід, досягаючи в чотири рази більшої кількості нормальної перирадикулярної тканини та підтримуючи аналіз високої роздільної здатності різних типів тканин», – пояснює старший автор доктор Мікіхіто Хаяші.
Після підтвердження ефективності своєї модифікованої моделі, дослідники вирішили вивчити вплив пародонтиту на експресію генів у різних типах тканин з часом, зосереджуючись на генах, пов'язаних із запаленням та диференціацією остеокластів.
Одним з ключових висновків дослідження було те, що експресія гена Il1rl1 була значно вищою в перирадикулярній тканині через п'ять днів після лігування. Цей ген кодує білок ST2 в ізоформах рецептора та пастки, який зв'язується з цитокіном під назвою IL-33, що бере участь у запальних та імунорегуляторних процесах.
Щоб глибше зрозуміти роль цього гена, команда дослідників індукувала пародонтит у генетично модифікованих мишей, у яких були відсутні гени Il1rl1 або Il33. Ці миші демонстрували прискорене запальне руйнування кісток, що підкреслює захисну роль шляху IL-33/ST2. Подальший аналіз клітин, що містять білок ST2 у його рецепторній формі, mST2, показав, що більшість із них походять з макрофагів.
«Макрофаги зазвичай класифікуються на два основні типи: прозапальні та протизапальні, залежно від їх активації. Ми виявили, що клітини, що експресують mST2, були унікальними тим, що вони одночасно експресували деякі маркери обох типів макрофагів», – прокоментував старший автор дослідження доктор Таканорі Івата. «Ці клітини були присутні в перирадикулярній тканині до початку запалення, тому ми назвали їх «резидентними макрофагами періодонтальної тканини»».
Разом результати цього дослідження демонструють здатність модифікованої тваринної моделі вивчати пародонтит у більш детальному масштабі, аж до біомолекулярного рівня.
«Ми пропонуємо можливість нового молекулярного шляху IL-33/ST2, що регулює запалення та руйнування кісткової тканини при захворюваннях пародонту, разом зі специфічними макрофагами в перирадикулярній тканині, які глибоко залучені до захворювань пародонту. Сподіваємося, що це призведе до розробки нових стратегій лікування та методів профілактики», – підсумовує старший автор дослідження, доктор Томокі Накасіма.
